摘要:盡管T細胞銜接器(TCE)在血液瘤領域已展現商業價值,全球首個獲批的TCEBlincyto年銷售額超12億美元,但與實體瘤相比,血液瘤的患者數量相對較小,僅占全部癌癥患者的10%左右,且賽道已十分擁擠。
盡管T細胞銜接器(TCE)在血液瘤領域已展現商業價值,全球首個獲批的TCE Blincyto年銷售額超12億美元,但與實體瘤相比,血液瘤的患者數量相對較小,僅占全部癌癥患者的10%左右,且賽道已十分擁擠。在更受資本青睞的實體瘤領域,TCE療法由于腫瘤微環境復雜、靶點異質性高、易引發細胞因子風暴等問題,仍面臨著巨大挑戰。
2025年美國癌癥研究協會(AACR)年會上,111家中國藥企攜246款創新藥成果亮相,眾多TCE產品大放異彩,涉及KLK2、LY6G6D、GPRC5D、BCMA、LILRB4、EGFR、CDH17、DLL3等多個靶點,尤其是維立志博全新設計的靶向DLL3的TCE雙特異性抗體-藥物偶聯物(TCE-ADC),為實體瘤領域的探索帶來了新思路。這是否預示著TCE在實體瘤領域即將進入高速發展快車道?
TCE:從設計藝術到科學落地
TCE技術的核心在于通過橋接T細胞上的CD3與腫瘤特異性抗原,有效聚集并激活T細胞,精準殺傷癌細胞。與CAR-T動輒數十萬美元的治療成本和ADC的化學毒性風險相比,TCE的“即用型”、無需基因改造、安全性更佳的優勢更為顯著。但在實體瘤領域,TCE技術的應用仍需攻克兩大難題:靶點選擇性不足與毒性控制失衡。
對此,各藥企基于不同的技術路徑與設計邏輯,持續迭代其TCE技術平臺的核心模塊,應對策略主要包括尋找合適的靶點、調整抗體靶向腫瘤的「價」數以增加對腫瘤的選擇性、合理控制靶向CD3抗體親和力以控制靶向殺傷和細胞因子釋放的平衡、Fc沉默等。
維立志博也通過獨創的LeadsBody?平臺對CD3 T-cell engager的分子設計進行多樣化修改,在不斷地升級優化中給出了TCE研發的“中國答案”:
●獨特的2:1非對稱結構,可精確控制T-cell engager與CD3和腫瘤標志物的結合強度,使其能夠有效激活T細胞,同時將細胞因子釋放最小化,減少T細胞衰竭。
●最優化的腫瘤相關抗原和CD3結合域的比例及親和力,將T-cell engager的作用導向腫瘤部位,最小化非靶向毒性。
●結構優化,精確定制結合臂的定位及空間排列,誘導T細胞有效殺死靶細胞,同時減少細胞因子分泌,展現出持久的抗腫瘤效果,減少T細胞耗竭的誘導。
LeadsBody?平臺的優越性讓維立志博在TCE技術上突破性平衡了T細胞激活與毒性控制的核心矛盾。理論上,其獨特設計的CD3 T-cell engager具有均衡的療效及安全性,治療窗口可能更大,可延長治療有效期,提高對血液瘤及實體瘤的療效。且這一理論已在臨床前研究和早期臨床試驗中得到充分驗證。
血液瘤領域,維立志博主要產品之一——用于治療多發性骨髓瘤的LBL-034 (GPRC5D/CD3雙特異性抗體),是目前全球臨床進度僅次于強生、中國臨床進度第一的靶向GPRC5D的CD3 TCE。根據公開資料,截至2025年2月26日,LBL-034劑量為400μg/kg時的客觀緩解率(ORR)為77.8%,達到非常好的部分緩解或更深程度緩解(≥VGPR)療效的比率為61.1%;劑量為800μg/kg時≥VGPR為100.0%,表現優于強生TALVEY?。且與TALVEY?類似藥物相比,LBL-034誘導的細胞因子釋放水平較低。美國血液學會年會(ASH 2024)上公布的I/II期臨床研究數據顯示,LBL-034在復發或難治性多發性骨髓瘤患者中未觀察到三級以上的細胞因子釋放綜合征(CRS)和免疫效應細胞相關神經毒性綜合征(ICANS)。就目前的臨床數據而言,LBL-034具有更強的療效、更好的安全性和更長更便利的給藥周期,有成為Best-in-Class的潛力。
實體瘤領域,用于治療MUC16高表達實體瘤,特別是卵巢癌、宮頸癌及子宮內膜癌等婦科癌癥的LBL-033 (MUC16/CD3雙特異性抗體),在靶向依賴性細胞毒性測定中,誘導T細胞的殺傷與另一款臨床階段候選藥物REGN4018的類似藥物相當,但細胞因子釋放較低。目前I/II期臨床試驗可用的數據中已觀察到LBL-033的初步療效信號及良好耐受性,劑量達到10mg/kg時未達到最大耐受劑量。
實體瘤:TCE療法的全球競速與突圍
2025 AACR已公布摘要中針對實體瘤的TCE創新藥超過30款,涉及DLL3、CDH17、HER2、MSLN、LILRB4等眾多靶點,適應癥覆蓋肺癌、結直腸癌、胃癌、卵巢癌、肝細胞癌等近20種實體瘤。雖然絕大部分研究處于臨床前,仍有Runimotamab(HER2xCD3)、ZW171(MSLN xCD3)等項目成功邁入臨床階段,標志著TCE技術正從血液腫瘤加速向實體瘤領域滲透。
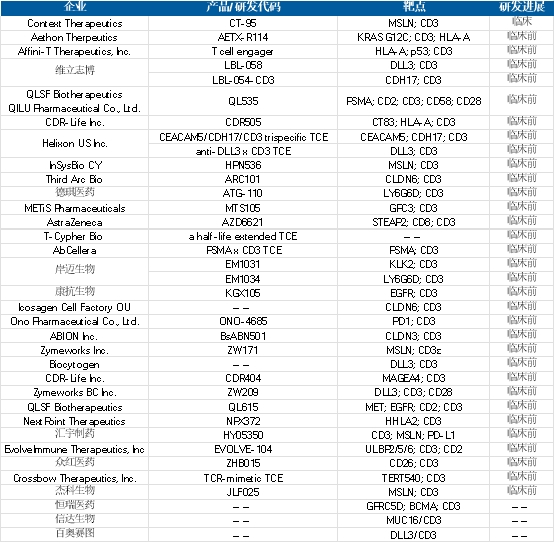
圖 2025 AACR線上摘要公布的TCE實體瘤項目(數據來源:醫藥魔方)
在這場全球競速中,約1/3的TCE實體瘤項目來自中國藥企,其中,維立志博憑借差異化策略嶄露頭角。一方面穩扎穩打,借助成熟的LeadsBody?平臺布局當下大熱的CDH17靶點,AACR摘要顯示,LBL-054(CDH17 xCD3)對CDH17 具有高親和力的同時不與其他CDH家族成員發生交叉反應,LBL-054介導的腫瘤細胞殺傷依賴于CDH17表達水平,對CDH17陰性細胞無細胞毒性作用。在體外和體內實驗中,LBL-054均展現出顯著的抗腫瘤活性。
另一方面,維立志博TCE-ADC的新玩法在業內備受關注。LBL-058由靶向DLL3×CD3的雙特異性抗體骨架與新型拓撲異構酶I抑制劑(TOP1i)載荷組成,利用具有自主知識產權的Linker-payload技術平臺開發。通過雙特異性抗體介導的T細胞激活與ADC的細胞毒效應協同,克服單一DLL3靶向療法的抵抗耐藥問題,直指小細胞肺癌(SCLC)治療痛點。AACR摘要顯示,LBL-058 高DLL3 親和力和低CD3 親和力的設計避免了對 T 細胞的潛在細胞毒性,不僅能誘導強效的TDCC和T細胞活化,還能選擇性地向DLL3陽性腫瘤細胞遞送細胞毒性載荷。體外實驗中,LBL-058在不同DLL3表達量的SCLC腫瘤細胞系中均展現出強效的殺傷。動物模型中,LBL-058在異種移植瘤模型中誘導持久的腫瘤消退。這是全球首個公開的TCE-ADC療法,展現了中國藥企在復雜技術路徑上的創新能力,也為TCE療法在實體瘤領域突圍提供了全新思路。
TCE矩陣:從數據到資本全面驗證研發實績
基于突破性設計和不斷優化迭代所打造的差異化優勢,維立志博的LeadsBody?平臺已經到了收獲期,實現從技術平臺到臨床價值的系統性轉化。目前,維立志博已構建起覆蓋血液瘤、實體瘤、自免疾病的TCE產品矩陣:
血液瘤領域,LBL-034(GPRC5D×CD3)有望成為首個靶向GPRC5D的國產TCE療法,用于治療多發性骨髓瘤;LBL-043(LILRB4×CD3)可能為急性髓細胞白血病提供高度差異化的治療方法。
實體瘤領域,LBL-033(MUC16×CD3)針對卵巢癌、宮頸癌等婦科腫瘤,是全球前二已進入臨床試驗的MUC16/CD3雙特異性抗體之一;LBL-054(CDH17×CD3)布局當下熱門靶點CDH17,劍指胃腸道惡性腫瘤;LBL-058(DLL3×CD3 TEC)更是開辟了TEC-ADC新賽道,有望解決小細胞肺癌耐藥難題。
自免領域,維立志博首創三抗LBL-051(CD19×BCMA×CD3),創下6.14億美元授權交易紀錄,一躍成為國內臨床前TCE管線最高交易金額。而與Aditum Bio的合作更進一步加速了其國際化戰略,通過NewCo模式整合全球研發資源,也為后續的商業化鋪平道路。
維立志博在2025 AACR年會上展示的研發成果和TCE管線進展,不僅驗證了其自主研發的LeadsBody?平臺在TCE技術領域的優越性,更以差異化布局為實體瘤治療提供了突破性解決方案。從血液瘤到實體瘤,從兼顧療效與安全性的科學設計到展現出優異抗腫瘤活性與耐受性的臨床驗證,從技術創新到國際化布局,維立志博憑借“硬核數據”躋身全球TCE研發第一梯隊,以領跑者的姿態推動腫瘤免疫治療格局的重塑。
全球領先的一站式視覺傳播平臺Canva可畫今日正式宣布在中國市場推出全新品牌企劃《心中所想,世界可見...
 2025-05-15
2025-05-15先是上個月前的濰坊風箏節,網上流傳的各種現場照片,讓人連連感嘆濰坊已經變成了年輕人的“抽象大舞臺”。
 2025-05-15
2025-05-15投資家網(www.51baobao.cn)是國內領先的資本與產業創新綜合服務平臺。為活躍于中國市場的VC/PE、上市公司、創業企業、地方政府等提供專業的第三方信息服務,包括行業媒體、智庫服務、會議服務及生態服務。長按右側二維碼添加"投資哥"可與小編深入交流,并可加入微信群參與官方活動,趕快行動吧。
